�Ϻ�2022��8��4�� /��ͨ��/ -- 2022��8��4�գ��۽��ڻ����ϸ�����Ƶ��Ϻ���ҫ����Ƽ�����˾�����¼��"��ҫ����"����������ҫ��������ϴ�ѧ����ҽԺ��������������CRISPR����༭���Ʀ�0/��0���ضȵ�ƶ�Ļ���Ŀǰ������Ѫ�����ѳ���2�������������������ѧϰ��ͬʱ�����ٴ�����ɹ����շ����ڹ��ʶ���ҽѧѧ���ڿ�Nature Medicine��Ӱ�����ӣ�87.241����Nature Medicine ���� ����
��Ϊ�������ڶ���ѧ���ڿ��Ļ���CRISPR����༭���Ʀ�0/��0���ضȵ�ƶ���ٴ��о������¹�������ϸ���ٴ����ݣ���Ϊȫ��ؽ����BRL-101���ƻ��ߵ���Ч�Ͱ�ȫ��������
��-���к�ƶѪ��һ���Ŵ�����Ѫ�Լ����������緶Χ���ձ����У�������ĵ�����֮һ�����ڹ����Ԧ�-�鵰������ȱ�����൱һ���ֻ�����Ҫ������Ѫ���ܴ��Ӷ�������Ѫ�����Ե��к�ƶѪ��TDT��������ѪҺ��Դ���������ϼ��ɱ��߰�������TDT���߽����ٲ��ֱ�����ά�ֹ淶��Ѫ�淶ȥ�����ƣ�����״̬���ǣ�TDT���ߵ����������Ե��ڷ�����ҡ�
�����о����ݣ������Ʒ��ɴ����õ�����Ч����ͨ������༭��ʽ�յ���-�鵰�ף�̥��Ѫ�쵰��HbF���ı����һ��������HBB����ͻ������Ħµ�ƶ�ļ���ǰ���IJ��ԡ���ҫ������ѧ���Ŷӽ��շ�����Nature Medicine������ϸ�����˸��Ʒ����ٴ����ݣ��������˻����Ʒ�����Ѫ�����Ԧµ��к�ƶѪ��TDT����ͯ�����еİ�ȫ�Ժ���Ч�������齫����༭��������Ѫ����ϸ����HSPCs����ֲ��������ͯ�������ڣ�����һ��������������ϣϣ����������Ϊ��0/��0��ϣϣ��������Ϊ�����ص�TDT���ͣ�����һ���������ƵĻ�����������������Ҳ����TDT����������Ͷ��ʱ������������̥��Ѫ�쵰�ֱ�ӻ���ʱ��2.55g/L��1.75g/L�ֱ����������һ�η��ӵ�149g/L��139g/L����Ѫ�쵰����Ҳ�ֱ�ﵽ��152g/L��140g/L���������ƺ�ʵ����������Ѫ��������16���£�������Ѫ�����Ķ���Ϊ��δ��Ѫ���������Ѫ�쵰�״ﵽ��90g/L�������������ƹ����У�����Ԥ������ض��Խ��ᣬδ�������صĸ�Ⱦ�����ֱ�����ֲ��52 ���40 ���Ժ������ͼ���������ߵĺ�ϸ������������Ѫ�쵰��ˮƽ�ڵ� 45 �����ҿ�ʼ�ȶ����ӣ��ڵ� 75 �����Ҵﵽ����ˮƽ��������ǰ������������������Ѫ�������ѳ���24���¡�
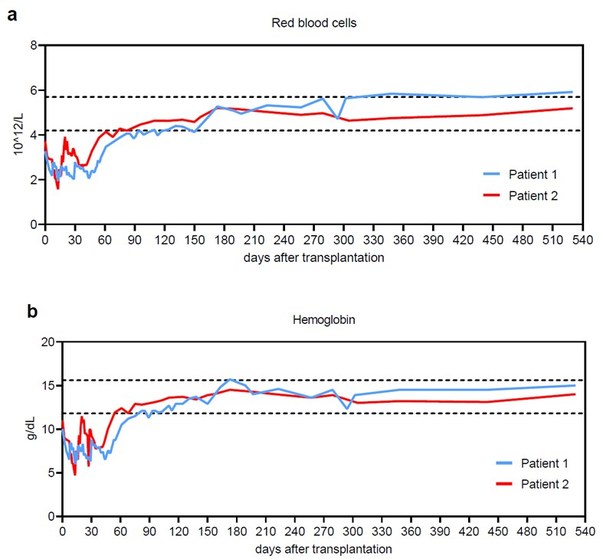
��ֲ���ϸ��������Ѫ�쵰�ױ仯����
�Ա༭���ؽ���PBMCs����ȱʧģʽ��̽���Է�����ʾ���ڽ������������ڣ�û�й۲쵽�쳣�Ŀ�¡����������ͬʱ���з���Ա�Ծ�����༭���ؽ���PBMCs�����˵�ϸ��RNA����ȫ�������δ�༭��༭��HSPC�����ѪҺ��ϵ��ת¼�飬����BCL11A��ϵ������ǿ�ӱ༭���ᵼ�·Ǻ�ϸ��������ת¼�仯������Ӱ��Bϸ���Լ�DCϸ���ķ���������ػ���ı�������Щ�������ʾ���Ʒ�û�����Եĸ�������
��֮�����о��ṩ������ʵ�� CRISPR/Cas9 �༭������HSPC����ֲ�ͳ���ֲ���ԭ��֤��������֤ʵ��̥��Ѫ�쵰��ˮƽ�ij����������Ը�����Ѫ�����Ԧ�-���к�ƶѪ����ʹ���ڦ�-�鵰����������ȫ�����Ƶ� ��0/��0 ������Ҳ����ˡ�
�������ҫ�����������Ŀ���������ʾ�������쳣�ļ�������������������Ч�����Ʒ���֮һ������������ؼ����ǻ��������켼���ĸ�Ч�Ͱ�ȫ��֮����ѡ��Ͱ�ҫ����������ǿ��а�ҫ�����ڻ�����켼�����������ڻ���༭���������Ѵ�����������ˮƽ������о���Ŀ�ijɹ�ʵʩ����������֤����ͬʱ����Ѫ��ϸ����ֲ�ɹ��ǻ������Ƴɹ��ıر�����������ٴ���ֲ�Ŷӵ���ֲˮƽͬ���ǻ������Ƴɹ��ıر���������Ŀ�ijɹ���չ�ǽ�����ǰ�ڸ�ˮƽ��Ѫ��ϸ����ֲ�����Ļ�����ȡ�õġ������ƽ���������������������ƺ�Ļָ�����dz����룬����Ϊ���¼������棺��һ��������Ѫ�dz��죬�������������ƺ�2�����ھ���������Ѫ������Ѫ�쵰�׳���������������Χ����Ȼ��Ѫ�쵰��������Ҫ�������յ�����������̥��Ѫ�쵰�ס��ڶ������������ڼ�û�з������صĺϲ�֢�����ƺ�Ҳû�����Ե����Ժϲ�֢�������ȫ���������Ҷ�������10cm����Ȼ����ȫ�Ժ���Ч�Լ���Ҫ����������ã�Ҳ��Ҫ��һ�������о���������֤��
��ҫ���ﶭ�³�����ҫ����˵�������������������ƺ�Ļָ��������������˵��һ�о������˹��ڻ���༭�������ٴ�ת�������ͻ���Գɹ����ӻ������ٴ�ת���о��Ѵ��ڹ�������ˮƽ��һ���棬���û���༭���Ʒ����Աȴ�ͳ�Ʒ���������Ϊ��Ч����ݺͰ�ȫ���ҳɱ����ͣ�������Ϊ���ݼ����ڵ��Ʒ�����һ���棬�������Ƶ�ƶ�ijɹ�������������úܶ��ƶ������ͥ������ϣ��������ͨ���ճ��������ƶ���ڵĴ������������߽Ӵ����Դ�Ҳϣ���ͺ�����δ����ֻ�Ǿ۽���ƶ����Ҳϣ������༭�Ʒ������Ƹ�������������Լ������ߡ�
Ŀǰ����ҫ�����������������Ļ��ڻ���༭��������Ѫ��ϸ��ƽ̨(ModiHSC®)�����Ʀ�0/��0���ضȵ�ƶ���ߵ��ٴ���������ȡ�������õ�Ч����ȫ����Χ���ѳɹ����������µ�ƶ����������Ѫ������������û��߰�����ʱ���ѳ���2�꣩ ��ֵ��һ����ǣ���ǰ��ҫ�����ڵ�ƶ�����ͻ���Գɹ���ѡ�뵽�ڶ��桶�й���ƶ������Ƥ�顷(2020)�����Ʒ������֣����Ҿ���2022��5��31�գ���ҫ�����"BRL-101������Ѫ����ϸ��ע��Һ"���ٴ������ù���ҩ���ҩƷ������ģ�CDE�������������ţ�CXSL2200236����δ�������һ��Ŀ���о��������佫��һ������35�꣬�����õ�ƶ��ֲ�����"�ϴ���Ⱥ��" -- ���估���������Ļ������档
��ҫ������Ϊһ����"�Ի���༭���촴�£�����ͻ�����Ʒ����츣ȫ����"Ϊʹ����ϸ������ҩ���Ͽ˷���ҵ���ݣ����ж�е��ս�Բ��֣�Ŀǰ�ڻ���༭���Ʀ�-���к�ƶѪ֢��PD1�ó��Dz�����������CAR-T���Լ�UCART����Ŀ���Ѿ�ȡ�������ٴ�Ч����δ�����Խ�ͨ�����ϵؼ����ƽ�����ҩ���ת������أ��Ӷ��츣�������к�ƶѪ���ڵ�ȫ���Ŵ������������������ߣ�
